19. Електрични потенциали в моделни системи. Дифузионен потенциал. Мембранен потенциал. Фазов потенциал.
Всички жизнени процеси се съпровождат с формирането на разлики в електричните потенциали между външната и вътрешната повърхност на клетъчните мембрани. За обяснението на физичната им природа нека разгледаме няколко случая на формиране на електрични потенциали в моделни системи.
19.1. Дифузионни потенциали.
Дифузионните потенциали възникват на границата на два разтвора на електролит с различна концентрация и различна подвижност на йоните.
Нека имаме съд, разделен на две части с пореста диафрагма, и от двете страни на съда имаме разтвор на NaCl с различна концентрация (Фиг. 19.1), като С1 е по-голяма от С2. В резултат на различната концентрация настъпва процес на дифузия. Поради различната подвижност на Na+ и Cl- йони, по-подвижните Cl- йони се движат по-бързо и изпреварват Na+ йони.
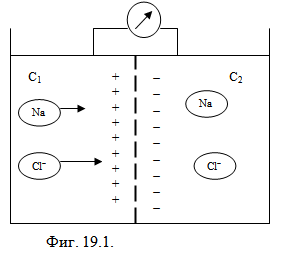 |
Дясната страна на мембраната се зарежда отрицателно поради по-голямото количество на Cl- йони, а лявата – положително поради по-голямата концентрация на Na+ йони. Създаденото електрично поле забавя хлорните йони и ускорява натриевите йони. След определено време се установява динамично равновесие на потоците на двата вида йони и се установява т.н. дифузионен потенциал. |
Големината на установилата се потенциална разлика от двете страни на порестата диафрагма се определя от формулата:
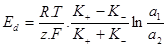
където R - универсална газова константа; T абсолютната температура; F - Фарадеево число; z - валентността на йона; К+ и К- - подвижността на йоните; а1 и а2 – активността на йоните в двете области.
Активността на йоните зависи от концентрацията и от един коефициент на активност, който отчита взаимодействието на йоните помежду им и с йонизирани групи на съседни молекули.
a=f.c, 0≤f≤1
Постоянната стойност на дифузионния потенциал се запазва кратко време, след което спада до нула с изравняване на концентрациите (Фиг. 19.2).
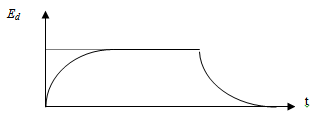
Фиг. 19.2.
Следователно за възникване на дифузионен потенциал е необходимо да се изпълняват едновременно две условия:
- да има разлика в концентрацията, т.е. да става дифузия;
- да има разлика в подвижността на противиположно заредения йон.
В биологични обекти дифузионния потенциал възниква при механично повреждане на клетъчната мембрана.
19.2. Мембранни потенциали.
Когато двете части на съд, в който има разтвор на електролит с различна концентрация са разделени с полупропусклива мембрана, през която един или няколко вида йони не могат да преминават, възниква потенциална разлика, наречена мембранен потенциал (Фиг. 19.3).
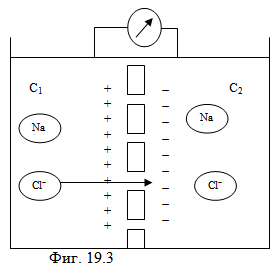 |
Полупропускливата мембрана в нашия случай пропуска само отрицателните йони, и не пропуска положителните. Такива мембрани обикновено се правят от йонообменни смоли с малки пори с фиксирани заряди в тях. Поради разликата в концентрациите хлорните йони ще дифундират през мембраната. Дясната страна на мембраната ще се зареди отрицателно поради по-голямото количество на Cl- йони, а лявата –– положително, поради по-голямата концентрация на Na+ йони. Когато двете части на съд, в който има разтвор на електролит с различна концентрация са разделени с полупропусклива мембрана, през която един или няколко вида йони не могат да преминават, възниква потенциална разлика, наречена мембранен потенциал (Фиг. 19.3). |
Създаденото електрично поле ще забавя хлорните йони. След определено време възникналия електричен градиент уравновесява концентрационния градиент и се установява постоянен мембранен потенциал. Големината му можем да определим като използваме формулата за дифузионния потенциал и отчитайки, че подвижността на единия вид йони е равна на нула.
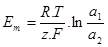
Например ако имаме разтвор на KCl с концентрации съответно 0.1 М и 0.01М от двете страни на полупропусклива мембрана, която пропуска само положителни йони, то от двете страни на мембраната при стайна температура ще се формира мембранен потенциал с големина приблизително 60 mV.
Мембранният потенциал след установяването му остава постоянен с времето за разлика от дифузионния потенциал (Фиг. 19.4).
Фиг. 19.4.
19.3. Фазови потенциали.
Фазов потенциал възниква на границата на две несмесващи се фази – например воден разтвор на електролит и мазнина. Нека положителните и отрицателните йони от електролита притежават различна разтворимост в неводна среда. Йоните с по-голяма разтворимост дифундират по-интензивно в неводната среда и я зареждат със сътветния знак по отношение на водната фаза. Големината на фазовия потенциал може да се определи с уравнението за дифузионния потенциал.
В клетките такива потенциали могат да възникнат в цитоплазмата, която представлява многофазна хетерогенна система.
20. Биопотенциал на покой. Уравнение на Голдман за големината на биопотенциала на покой.
Всички жизнени процеси се придружават от появата на електрични напрежения, свързани с разлика в електричните потенциали на две точки в една клетка или тъкан. Исторически се е наложил терминът биопотенциал, въпреки че физически трябва да се използва термина бионапрежение.
За произхода на биопотенциалите има предложени различни теории, но най-добре теоретично и експериментално е обоснована мембранната теория, според която биопотенциалите са мембранни потенциали, възникнали вследствие на асиметричното разпределение на йоните между клетката и обкръжаващата я среда, поддържано чрез механизма на астивен пренос. Експерименталното изследване на биопотенциалите се прави с помощта на микроелектроди, поставени съответно във вътреклетъчната и извънклетъчната течност. Особено удобен обект за изследване е аксонът на нервни клетки на калмар, който може да достичне диаметър 1 милиметър.
Разликата в потенциалите между вътрешната и повърхност на клетъчната мембрана, измерена в състояние на физиологичен покой се нарича биопотенциал на покой. При всички случаи потенциалът на вътрешната течност е отрицателен спрямо потенциала на външноклетъчната течност, като разликата в потенциалите е най-често между 50 и 100 mV при различните видове клетки.
Клетъчната мембрана е проницаема главно за 3 вида йони – Na+, K+ и Cl- йони, които се съдържат както в клетката, така и във външната среда, но в различни концентрации (Фиг. 20.1).
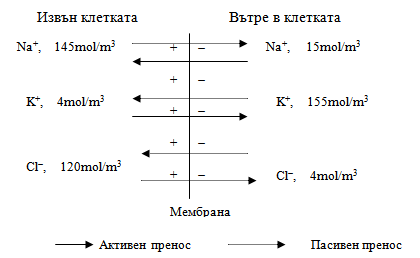
Фиг. 20.1
Общият потенциал, който се формира в резултат на разликата в концентрациите на тези йони между клетката и извънклетъчната среда се дава с обобщеното уравнение на Голдман:
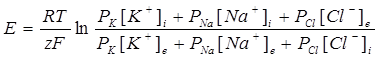
където PK, PNa и PCl са коефициентите на проницаемост на мембраната за съответните йони, [K+], [Na+] и [Cl-] са концентрациите им в клетката и извън нея. Индексът i означава, че стойността се отнася за концентрацията вътре в клетката, е – съответно извън клетката. Коефициентите на проницаемост за гигантско нервно влакно на сепия са съответно: PK : PNa : PCl = 1 : 0.04 : 0.45
Тъй като мембраната е много тънка, разлика в потенциала от 70 mV означава, че интензитета на електричното поле ще бъде много голям. При дебелина на мембраната приблизително 9 nm, ще получим:
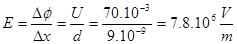
Следователно тънката клетъчна мембрана издържа без пробив електрично поле с огромна интензивност – до 109 V/m според някои автори.
Установено е, че от 30 до 40% от енергийните потребности за поддържане на живота отиват за поддържане на електричните градиенти в мембраните на клетките.
21. Възбудимост. Характеристики на възбудните процеси.
Биопотенциалите са свързани и със способността на живите организми да отговарят на различни дразнения. Сигналите от рецепторите до главния мозък, както и командите от главния мозък до съответните органи се предават чрез импулсни изменения на биопотенциалите на нервните е мускулните влакна. Тези изменения на биопотенциалите се наричат акционни потенциали.
Възникването на акционни биопотенциали е свързано с процеса възбудимост. Възбудимост е отговорът на живата система на външно въздействие чрез изменение на характера или интензивността на протичащите в нея процеси.
Дразненето е прагова реакция. Когато дразненето превишава определена стойност, наречена праг на дразнене, отговорът е винаги еднакъв – възбуда. Възникващият акционен потенциал не е пропорционален на дразненето, т.е. имаме реакция от типа “всичко или нищо”.
Прагът на дразнене се определя количествено с праговата енергия на дразнене. Ако за дразнене се използва електричен ток, то праговата енергия на дразнене можем да изразим чрез големината на действащия електричен ток. Следователно големината на праговият ток е обратно пропорционална на времето на действие на токовия импулс. За да се получи възбуда при краткотрайно дразнене и необходим по-силен ток, а при по-слаб ток той трябва да действа по-дълго време. Графично зависимостта на праговият ток от продължителността на действие на импулса има вида, представена на фиг. 21.1. Съществува една минимална стойност на големината на тока Imin, под която токовият импулс не може да предизвика възбуда, колкото и да е продължителен. Този минимален ток се нарича реобаза (Р). Продължителността на токовия импулс, който предизвиква дразнене при големина на тока, равна на удвоената реобаза, се нарича хронаксия (Х).
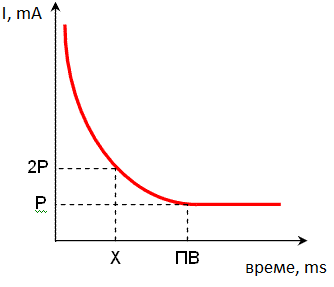
Фиг. 21.1. Зависимост на праговият ток от продължителността на действие на импулса.
При възбудните процеси е в сила законът за сумиране на енергията на дразнене. Две дразнения с подпрагова енергия предизвикват възбуда, ако сумата от енергиите им превишава праговата енергия.
22. Акционен биопотенциал. Механизъм на формиране на акционния биопотенциал. Разпространение на акционния потенциал по повърхността на клетката. Ток на действие. Скорост на разпространение.
22.1. Механизъм на формиране на акционния биопотенциал.
При възбуда, потенциалната разлика между клетката и средата, възникваща при възбуда на клетката, се нарича акционен биопотенциал или потенциал на действие. Възбуденият участък се деполяризира – т.е. става положително зареден отвътре и отрицателно зареден отвън. Следователно в мястото на възбуждане става преразпределение на йони (Фиг. 22.1).
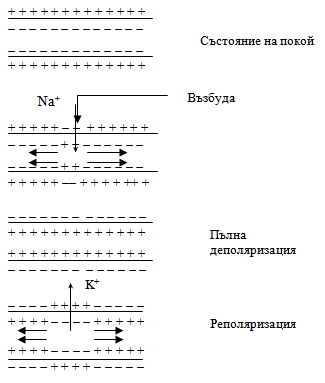
Фиг. 22.1.
Изменението на потенциала на цитоплазмата с течение на времето при възбуда е представено на фиг 22.2. Потенциалът на покой за аксон на калмар има стойност около –50 mV спрямо външната повърхност на клетъчната мембрана. При възбуда мембранният потенциал намалява до нула и след това нараства до +40 mV. Това става за части от секундата (0.5 - 4 ms).
Какъв е механизмът на получаване на акционния биопотенциал? В момента на възбудата проницаемостта на мембраната за Na+ йони се увеличава 500-1000 пъти и става дифузия на Na+ йони от извънклетъчната среда вътре в клетката, тъй като концентрацията на Na+ йони е много по-голяма извън клетката. Потокът на Na+ йони намалява постененно отрицателния заряд на цитоплазмата и вътрешната повърхност на клетъчната мембрана се зарежда положително спрямо външната. В този момент проницаемостта на мембраната за K+ и Cl-- йони не се променя. При един акт на възбуждане през 1 mm2 от повърхността на мембраната преминават около 20 000 Na+ йони.
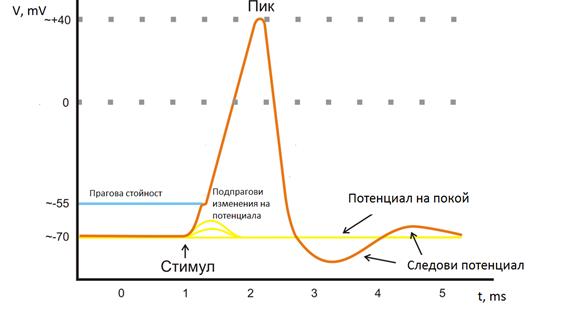
Фиг. 22.2.
Стойността на акционният потенциал се определя основно от Na+ йони и може да се пресметне от уравнението на Голдман 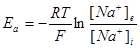
След деполяризацията на мембраната, електричното поле препятства по-нататъшното навлизане на Na+ йони в клетката. След това се повишава проницаемостта на мембраната за К+ йони и започва дифузия на К+ йони от клетката навън поради концентрационния градиент и този процес възстановява биопотенциала на покой. Основна роля при формирането на акционния потенциал играе пасивния пренос и затова става толкова бързо. Пълното изменение на потенциала на клетъчната мембрана при възбуда ще бъде 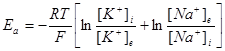
Процесите на формиране на акционния потенциал са свързани с отваряне и затваряне на йонни канали в мембраните. При генериране на импулса се отваря Na канал, след това се открива К канал, който възстановява биопотенциала на покой – т.е. настъпва реполяризация.
22.2. Разпространение на акционния потенциал по повърхността на клетката. Ток на действие. Скорост на разпространение.
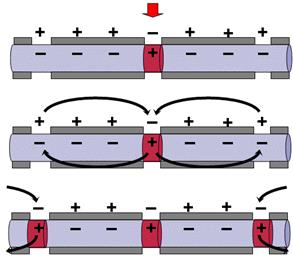
Акционният биопотенциал се разпространява по повърхността на клетката, понеже между възбудените и невъзбудените участъци съществуват потенциални разлики. Това предизвиква дразнене на съседните участъци (Фиг. 22.3). По този начин възбудата се предава по клетката чрез локален ток, наречен ток на действие.
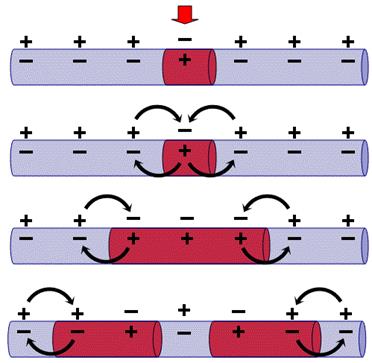
Фиг. 22.3. Механизъм на разпространение на акционния потенциал.
Възбудата преминава от една клетка към друга чрез функционални контакти, наречени синапси. Скоростта на разпространение на тока на действие може да бъде от 0.5 до 130 m/s и зависи от диаметъра на нервното влакно и от това дали е покрито с миелинова обвивка или не. Аксоните по отношение на електричните свойства наподобяват кабел с проводяща сърцевина и изолираща обвивка. Съпротивлението на изолацията е много голямо, а на аксоплазмата – малко. Ако в мястото на възбуждане потенциалът е Еа, то на разстояние l напрежението на мембраната ще бъде 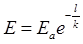
Коефициентът k е равен на 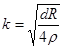 . Във формулата d е диаметъра на влакното, R повърхностното съпротивление на мембраната, ρ специфичното съпротивление на аксоплазмата. Колкото е по-голям коефициентът к, толкова по-малко е затихването на сигнала. Тъй като ρ и R са приблизително еднакви за всичко организми, то увеличаването на к може да стане чрез увеличаване на диаметъра на аксона. Затова при калмарите аксоните им достигат гигантски размери. Това осигурява достатъчно бързо провеждане на нервните импулси и следователно бърза реакция на външни дразнители.
. Във формулата d е диаметъра на влакното, R повърхностното съпротивление на мембраната, ρ специфичното съпротивление на аксоплазмата. Колкото е по-голям коефициентът к, толкова по-малко е затихването на сигнала. Тъй като ρ и R са приблизително еднакви за всичко организми, то увеличаването на к може да стане чрез увеличаване на диаметъра на аксона. Затова при калмарите аксоните им достигат гигантски размери. Това осигурява достатъчно бързо провеждане на нервните импулси и следователно бърза реакция на външни дразнители.
Друг механизъм за увеличаване на скоростта на распространение на тока на действие е миелиновата обвивка на аксоните (Фиг. 22.4). Миелиновата обвивка е разделена на сегменти с дължина от 1 до 3 mm, а между сегментите има свободни участъци с дължина около 1 mm. Те се наричат възли на Ранвие. Тъй като миелиновата обвивка има голямо съпротивление, то по повърхността и не могат да протичат токове. При възбуда на един възел възникват токове между тъх и другите възли. Загубите на енергия при разпространение на сигнала по миелизирано влакно са много по-малко, отколкото по немиелизирано влакно. Скоростта на разпространение достига до 130 m/s. При блокиране на възлите на Ранвие с анестезиращи средства, съпротивлението на аксона нараства и преминаването на сигнала по нервното влакно се забавя или съвсем се прекъсва. По този механизъм функционират някои от упойките.
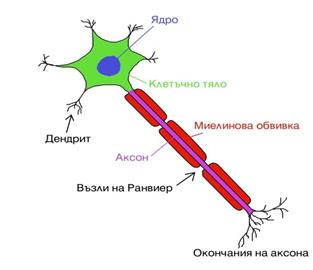
Фиг. 22.4. Схема на аксон с миелинова обвивка и начина на разпространение на акционния потенциал.
23. Електрична активност на сърцето. Електрокардиография. Електрична активност на мускулите и мозъка. Електроенцефалография и електромиография.
Изучаването на акционните биопотенциали, възникващи в резултат на дейността на различни вътрешни органи на животните и човека като сърцето, мозъка, мускулите и др. има важно диагностично значение и може да покаже физиологичното и функционалното им състояние. Регистрацията на биопотенциалите на тъканите и органите с диагностична и изследователска цел се нарича електрография. В зависимост от органа, електричната активност на който се отчита, говорим за:
- електрокардиография (ЕКГ) – регистрация на биопотенциалите, възникващи в сърдечния мускул при неговото възбуждане;
- електроенцефалография (ЕЕГ) – регистрация на биопотенциалите на главния мозък;
- електромиография – регистрация на биоелектричната активност на мускулите.
Директното измерване на акционните потенциали изисква въвеждане на електрод в съответното нервно влакно и не е възможно да се използва за рутинни изследвания. За щастие електроди, поставени на повърхността на кожата, могат да регистрират малки сигнали, свързани с електричната активност на сърцето и главния мозък. Тези сигнали са от порядъка на 50mV или около 0.1 процент от стойността на потенциалите на повърхността на съответния орган. Въпреки това тези сигнали могат да се усилят и да се измерят.
В повечето случаи се отчитат разликите в биопотенциалите, регистрирани между две точки от повърхността на тялото. Тази разлика в биопонапрежението между две точки от повърхността на тялото се нарича отвеждане. Кривата на зависимостта на бионапрежението от времето се нарича електрограма от съответния вид – електрокардиограма, електроенцефалограма и т.н.
23.1. Електрокардиография.
Първият опит за регистриране на електрични явления в сърцето е направен от Валер през 1889 г. Точното измерване на кардиограма е осъществено от Айнтхофен, а през 1903 г. той създава и първия електрокардиограф. Той определя и буквите P, Q, R, S и T за означаване на отделните части на кардиограмата. За своето откритие Айнтхофен получава Нобелова награда по физиология и медицина. По този начин се поставя основата на елекрокардиографията като един от най-използваните методи за диагностика.
Биопотенциалите на сърцето възникват при възбуда на нервно-мускулния му апарат. За един сърдечен цикъл възбудата се разпространява по сърцето с определена последователност, като най голяма разлика в потенциалите възниква между основата и върха на сърцето по направление на анатомичната му ос. Тя се нарича електрична ос на сърцето. Сърцето може да разглеждаме като електричен дипол, разположен в проводяща среда, с диполен момент рс. За един сърдечен цикъл вектора на диполния момент се променя както по големина, така и по посока, тъй като възбудата обхваща последователно различните части на сърцето.
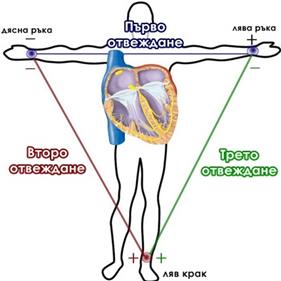
Нека имаме 3 електрода, разположени на дясната и лявата ръка и левия крак, които образуват равностранен триъгълник, като се отчитат потенциалните разлики между всеки две от трите точки. Всяка от измерените потенциални разлики е пропорционална на проекцията на електричния вектор на сърцето върху съответната страна на получения триъгълник, както е представено на фиг.23.1.
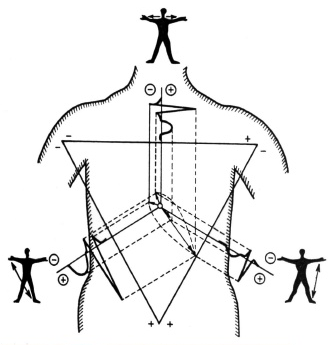
Фиг. 23.1. Проекции на електричния вектор на сърцето.
Видът на получената крива зависи от функционалното състояние на сърцето. Една кардиограма има приблизително следния вид (Фиг. 23.2).
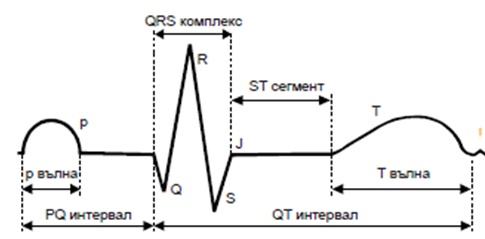
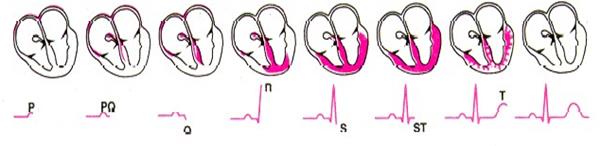
Фиг. 23.2.
P – вълната е свързана със съкращаване на предсърдията, пикът QRS е свързан с началото на съкращение на камерите, а Т вълнат се регистрира в края на съкращението на камерите. При един и същ начин на отвеждане височините на характерните зъбци P, QRS и T и разтоянието между тях зависят от функционалното състояние на сърцето.
Сега в кардиологията са въведени 12 стандартни отвеждания. Шест от тях I, II, III, aVR, aVL и aVF са от крайниците и се наричат периферни, а останалите 6, означавани от V1 до V6 са от лявата предна половина на гръдния кош и се означават като прекордиални (Фиг. 23.3).
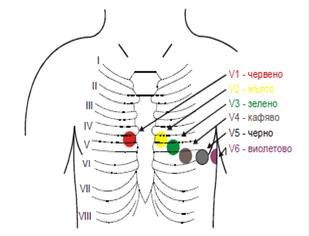
Фиг. 23.3. Място за поставяне на електроди за кардиограма.
Образователна игра, свързана с електрокардиограмите, се намира в сайта на нобеловия комитет http://www.nobelprize.org/educational/medicine/ecg/index.html.
23.2. Електроенцефалография
Зависимостта от времето на биопотенциалите на мозъка, отведени от повърхността на черепа или непосредствено от мозъка, се нарича електроенцефалограма (Фиг. 23.4).

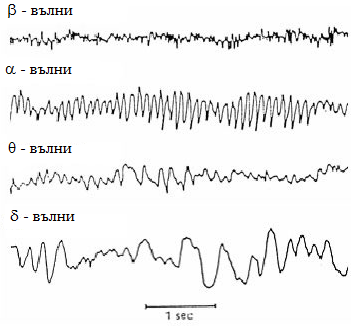
Фиг. 23.4.
Една от особеностите на ЕЕГ – кривите е наличността на ясно изразени трептиеия с определени честоти:
- α - вълни – с честота от 8 до 13 Hz и приблизително синусоидална форма
- β - вълни – с честота от 14 до 50 Hz
- δ- вълни – с честота от 0.5 до 4 Hz
- θ- вълни – с честота от 5 до 7 Hz
ЕЕГ зависи от състоянието на съзнанието на пациента и носи информация за дейността на централната нервна система, за наличието на органични изменения в мозъка, локализациите на увреждания и т.н. Нискочестотните d и q вълни обикновено са показатели за патологични изменения.
23.3. Електромиография.
Електричната активност на мускулите и инервиращите ги нерви може да се регистрира чрез въвеждане на електроди в мускулната маса (Фиг. 23.5). Електромиографията има голяма диагностична стойност и позволява да се открият патологични изменения в мускулните влакна и инервиращите ги нерви.

Фиг. 23.5. |
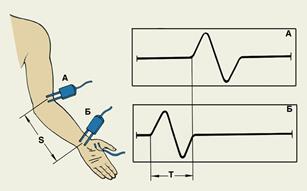 Методика за определяне на скоростта на провеждане на импулса. А и Б – точки на стимулация,В – отвеждащ електрод, S – разстояние между електродите |




