Ключови думи: биологично окисление, редокс-системи, окислително и субстратно фосфорилиране, дихателна верига
Цели:
- Да се изясни същността и значението на биологичното окисление.
- Да се научат редокс-системите с биологично значение.
- Да дадат определения за окислително и сустратно фосфорилиране.
- Да се изясни значението на субстратното фосфорилиране.
- Да се изясни значението на окислителното фосфорилиране.
- Да се изясни структурата на дихателната верига.
Въведение
Метаболизмът е целенасочена клетъчна активност, с три основни функции – енергетична (снабдява клетките с енергия), пластична (синтез на макромолекули) и специфична (синтез и разграждане на биомолекули, със специфични клетъчни функции). Метаболизмът е високо координиран и обезпечаван от участието на голям брой взаимносвързани ензимни системи, включващ два неразривно свързани процеса анаболизъм и катаболизъм.
Анаболизъм. Това е биосинтез на белтъци, полизахариди, липиди, нуклеинови киселини и други макромолекули от техни предшественици, съпровожда се с разход на енергия. Източник на енергия е АТФ. За биосинтезата на някои вещества, като мастни киселини и холестерол, са необходими богатите на енергия атоми водород, чийто източник се явява НАДФН. Молекулите НАДФН се образуват в реакциите на окисление на глюкозо-6-фосфата в пентозния цикъл и оксалацетата.
Катаболизъм. Процес на окисление и разграждане на сложни органични молекули до по-прости крайни продукти, като се освобождава енергията включена в тях. Голяма част от освободената енергия се разсейва под формата на топлина, малка част се улавя от коензимите на окислителните реакции НАД и ФАД, и веднага се използва за синтеза на АТФ.
Атомите водород отделени в реакциите на окисление, могат да се използват от клетката само по два начина:
- в анаболитни реакции в състава на НАДФН;
- за образуване на АТФ в митохондриите при окисление на НАДН и ФАДН2.
Катаболизма условно се разделя на три етапа:
- Първи етап – протича в лумена на червата или в лизозомите при разграждане на ненужните молекули. Освобождава се около 1% от енергията включена в молекулата, която се разсейва под формата на топлина;
- Втори етап – веществата, образувани при вътреклетъчния хидролиз или проникващи от кръвта в клетката се превръщат в пируват, ацетилна група (в състава на ацетил-S-КоА), или в някои малки органични молекули. Локализацията на този етап е цитозола и митохондриите. Част от освободената енергия се разсейва като топлина и около 13% се съхранява във вид на макроергични връзки на АТФ.;
- Трети етап – всички реакции на този етап протичат в митохондриите. Ацетил-S-КоА се включва в реакциите на ЦТК и се окислява до СО2. Отделените атоми водород редуцират НАД и ФАД. След това НАДН и ФАДН2 пренасят водорода до дихателните ензими, разположени на вътрешната мембрана на митохондрия. В тях протича окислително фосфорилиране, при което се образува вода и АТФ. Част от отделената енергия се разсейва като топлина и около 46% се съхранява като макроергични връзки на АТФ и ГТФ.
В живите организми, както и в неживата природа, окислението (отделяне на електрони) винаги е свързано с редукцията (приемане на електрони). Биологичното окисление е спрегнато с окислителното фосфорилиране, чрез което енергията на химичните връзки от различни вещества се освобождава и акумулира в макроергични съединения, за да се използват при необходимост, за осигуряване на жизнените процеси.
Молекулите НАД.Н и ФАД.Н2, образувани в реакциите на окисление на въглехидрати, мастни киселини, алкохоли и аминокиселини, постъпват в митохондриите, където ензимите на дихателните вериги осъществяват процес на окислително фосфорилиране. Окислителното фосфорилиране е многоетапен процес, протичащ във вътрешната мембрана на митохондриите, съпроводен със синтеза на АТФ. При окислението в дихателни вериги се отделят значителни количества енергия, която се акумулира в АТФ. Окислителното фосфорилиране в дихателната верига дава около 75%, а субстратното фосфорилиране около 25% от АТФ в клетките.
Дихателната верига е сложно организирана и специализирана система разположена във вътрешната митоходрийна мембрана със следните функции: да събира редуциращи еквиваленти от различни субстрати, да ги пренася към О2 (окисление) и да акумулира отделената при окислението енергия като синтезира АТФ (окислително фосфорилиране).
Клетките, които използват кислород като електронен акцептор за получаване на енергия, имат аеробен метаболизъм, а тези които не използват кислород, имат анаеробен метаболизъм.
9.1. Биологично окисление в клетката. Редокс-системи с биологично значение
9.1.1. Биологично окисление
Биологичното окисление се отличава със следните особености:
- катализира се от оксидоредуктази (двукомпонентни ензими), които действат съвместно с редокс-системи, които го ускоряват и му придават специфичност, и възможност за регулация. Отделените от субстрата водород или електрони се пренасят върху краен акцептор. При аеробни условия краен акцептор е кислородът, който се редуцира до вода. При анаеробни условия краен акцептор е друго вещество, напр. пируват, който се редуцира до лактат, или ацеталдехид, който се редуцира до етанол.
- водородът или електроните, отделени от субстратите на биологичното окисление достигат до кислорода или друг краен акцептор, чрез поредица от реакции под действие на ензими с техните редокс-системи подредени по нарастващ редокс-потенциал в електронпренасяща, дихателна верига.
- енергията се отделя на порции, а не експлозивно и се съхранява в макроергични връзки. Само първата порция остава пряко свързана с окислението на субстрата - т.е. в субстратната верига. Това постепенно (на порции) освобождаване на енергията в стъпалата на дихателните вериги позволява максимална част от нея да бъде превърната в макроергични съединения - в дихателните вериги се получават няколко мола АТФ при окисление на 2 Н атома, отделени от субстрата.
В клетката протичат четири основни процеса, освобождаващи енергия от химичните връзки при окисление на веществата и нейното съхранение чрез образуване на АТФ:
- Гликолиза (втори етап на биологично окисление) – окисляване на молекулата на глюкозата до две молекули пируват, при което се образуват 2 молекули АТФ и НАДН. След това пирувата в аеробни условия се превръща в ацетил-SКoA, в анаеробни условия – в млечна киселина.;
- β – Окисление на мастните киселини (2 етап биологично окисление) – окисление на мастните киселини до ацетил-SKoA, образуват се НАДН и ФАДН2. Молекули АТФ директно не се синтезират.
- Цикъл на трикарбоновите киселини (ЦТК, 3 етап биологично окисление) – окисление на ацетилната група (в състава на ацетил- SKoA), или други кетокиселини до въглероден диоксид. Образуват се 1 молекула ГТФ (еквивалент на АТФ), 3 молекули НАДН и 1 молекула ФАДН2.
- Окислително фосфорилиране (3 етап на биологично окисление) – окисляват се НАДН и ФАДН2, получени в реакциите на катаболизъм на глюкозата, аминокиселините и мастните киселини. При това ензимите на дихателната верига във вътрешната мембрана на митохондриите обезпечават образуването на основната част на клетъчната АТФ.
Основен начин за получаване на АТФ в клетката е окислителното фосфорилиране, протичащо в структурите на вътрешната мембрана на митохондриите. При това енергията на атомите на водорода в молекулите на НАДН и ФАДН2, образувани в гликолизата, ЦТК, окислението на мастните киселини се преобразуват в енергия на макроергичните връзки на АТФ. Адениловата система (АТФ/АДФ) е най-често използваният посредник между екзергоничните и ендергонични процеси протичащи в клетката. Синтезата на АТФ от АДФ и неорганичен фосфат за сметка на енергия отделена от окислителен процес се означава като окислително фосфорилиране.
Друг начин на получаване на АТФ в клетката (фосфорилиране на АДФ до АТФ), е субстратното фосфорилиране. Този начин е свързан с предаване на макроергичен фосфат или енергията на макроергичната връзка на кое да е вещество (субстрат) на АДФ. Такива субстрати са метаболитите от гликолизата (1,3-дифосфоглицерат, фосфоенолпируват), от цикъла на трикарбоновите киселини (сукцинил-SKoA) и креатинфосфат. Енергията освободена от хидролиза на техните макроергични връзки се използва за фосфорилиране на АДФ до АТФ. Макроергични връзки са тези, при чието хидролитично разграждане ∆Go' е най-малко 30 kJ/mol до 70 kJ/mol. При хидролитично разграждане на нормоергични връзки ∆Go' е от 8 до 21 kJ/mol.
При биологичното окисление, водородът или електроните отделени от субстратите, достигат крайния акцептор постепенно и многостъпално, минавайки в поредица от реакции, катализирани от ензими с техните редокс- системи с последователно нарастващи редокс-потенциали. Биологичното окисление се катализира от оксидоредуктази (I група ензими). Оксидоредуктазите се разделят на четири групи: дехидрогенази, оксидази, оксигенази и хидроксипероксидази.
Анаеробни дехидрогенази - катализират съвместно с никотинамидни или флавинови редокс-системи. Тук спадат и анаеробните транселектронази (цитохроми). Всички ензими от тази голяма група са анаеробни, т. е. не могат да използват кислород като акцептор на водорода. Специфични са по отношение на субстрата и участват както в субстратното окисление, така и в дихателната верига. В зависимост от редокс-системата, с която действат, има дехидрогенази с никотинамидни редокс-системи (катализират пренос на 1Н и 1е-, хидриден йон). Дехидрогенази с флавинови редокс-системи. Обикновено дехидрогеназните реакции са обратими поради малката разлика в редокспотенциала между субстрата и редокс-системата. Никотинамидните редокс-системи са слабо свързани с апоензима, докато връзката между него и флавиновите редокс-системи е много по-здрава, дори ковалентна в някои случаи. Анаеробни транселектронази, катализират пренос на един електрон. Тук спадат цитохромите от дихателната верига (без цитохром аа3). Транселектронази са също и цитохромите в електрон-пренасящите вериги в ендоплазмения ретикулум.
Аеробни оксидази - кислорода е акцептор на водорода отделен от субстратите, при което се образува вода или водороден прекис. Цитохром с оксидаза (цитохром аа3), съдържа хем като простетична група и медни йони, краен ензим в дихателната верига, предава електроните от цитохром с към кислорода, при което заедно с протони се образува вода:
4 цит.с (Fe2+) + 4Н+ + О2 → 2 h3O + 4 цит.с (Fe3+)
Останалите оксидази, наричани също аеробни дехидрогенази, не са свързани с дихателните вериги, съдържат най-често ФМН или ФАД като простетични групи, т.е. са флавопротеини. Катализират пренос на два водородни атомa от субстрата директно към кислород, при което се получава водороден прекис вместо вода. Отделената при окислението на субстрата енергия се разсейва като топлина. АТФ не се получава. Към оксидазите- флавопротеини спадат аминоацидо оксидази, ксантин оксидаза, алдехид дехидрогеназа, глюкозо оксидаза.
Оксигенази: Монооксигенази (хидроксилази), катализират вмъкването на един атом кислород в субстрата, при което се получава алкохолна или фенолна група. Другият кислороден атом се редуцира до вода от друг донатор на водород:
R-H + O2 + R1-h3 → R-OH + Н2О + R1
Тези ензими са част от електрон-пренасящите вериги в ендоплазмения ретикулум в черния дроб, хидроксилират неспецифично лекарства и други чужди за клетката вещества с цел обезвреждане. Митохондрийните хидроксилазни системи катализират стереоспецифични хидроксилирания в биосинтезите на стероидни хормони, витамин D, жлъчни киселини и др.
Диоксигенази, вмъкват два атома кислород в ароматни пръстени (пероксид), последвано от окислително разтваряне на пръстена, участват при разграждане на аминокисeлини.
Хидрокспероксидази (пероксидази, каталаза) - обезвреждат токсични прекиси и получаваните от тях свободни радикали, които увреждат белтъци, нуклеинови киселини, мембрани.
9.1.2. Редокс-системи с биологично значение
Към редокс-системите с биологично значение спадат:
Никотинамидни. Никотинамидаденин динуклеотид (НАД+/НАДН+Н+) и никотинамидаденин динуклеотидфосфат (НАДФ+/НАДФН+Н+), нисък редокс- потенциал, кофактори на анаеробни дехидрогенази лесно дехидрогенират стотици различни субстрати. НАДН предава водорода на дихателната верига, а НАДФН на редукционни биосинтези. При необходимост специален ензим трансхидрогеназа може да пренасочва големи потоци водород от катаболитно в анаболитно направление и обратно, тъй като катализира обратимата оксидо-редукция между двете никотинамидни редокс-системи:
трансхидрогеназа
НАДФН + НАД+ ↔ НАДФ+ + НАДН
Флавинови. Флавинмононуклеотид (ФМН) и флавинадениндинуклеотид (ФАД). Характеризират се с по-висок редокс-потенциал от никотинамидните и са коензими или простетични групи на свързаните с дихателната верига дехидрогенази и на някои оксидази. Освен напълно редуцирана и окислена форма, имат и семихинонова форма, с което улесняват прехода от дву- към едноелектронен пренос. Тези редокс-системи пренасят два Н атома (електрони), като се минава през междинна семихинонова форма, която е стабилен свободен радикал. Кислородът, крайният акцептор на електрони в аеробните организми, може да приема само единични електрони (несдвоени), а от метаболитите електроните се отделят по двойки.
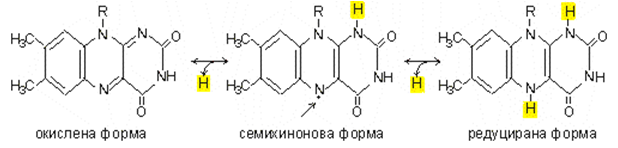
Фигура 131. Семихиноновата форма осъществява преход между дву- и едноелектронен пренос - флавинова редокс-система
Редокс-системи с хинонова структура. KoQ (убихинон, англ. ubi- повсеместен, фиг.132), хидрофобен мобилен компонент на дихателната верига, редуцираната и окислената форми не са свързани с белтък. Семихиноновата форма е прикрепена към Q-свързващ белтък във вътрешната митохондрийна мембрана.
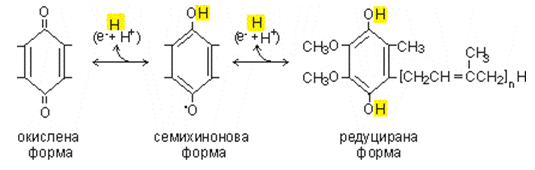
Фигура 132. Редуцирана, семихинонова и окислена форми на КоQ (убихинон). n - брой на изопреновите остатъци. При човек n=10.
Убихинон участва в преноса на електрони между неподвижно вградените компоненти на дихателната верига, а именно между флавопротеините и цитохромите (фиг.135). Участва и в изпомпването на протони от матрикса към междумембранното пространство посредством т.н. Q-цикъл.
Метал-съдържащи редокс-системи - железни и медни йони, свързани към белтъчен компонент, Fe-S белтъци и различни хемове - простетични групи на цитохроми.
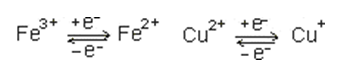
Осъществяват едноелектронен пренос в дихателната верига и в електронопреносителни вериги в ендоплазмения ретикулум. В различните цитохроми хемовете се различават по страничните заместители и връзки с белтъчната съставка. Общото за всички хемове в цитохромите е, че валентността на Fe-йон се мени от +2 до +3 и обратно и така се осъществява пренос на електрони. Това е съществена разлика от непроменящата се валентност на Fe2+ - йон в хема на хемоглобин и миоглобин, които пренасят кислород, а не електрони.
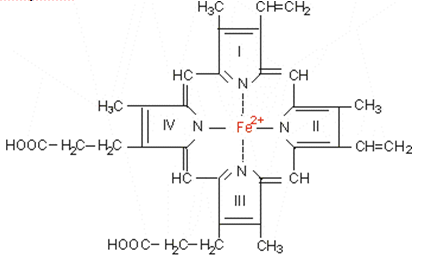
Фигура 133. Структура на хема на цитохром b (редуцирана форма)
Тиолови редокс-системи. Тук спадат липоевата киселина и глутатион, които в окислената си форма съдържат дисулфиден мост, а в редуцираната - сулфхидрилни групи. Глутатион е добър редуктор и наред с НАДФН участва в процеси на обезвреждане на токсични радикали.
Аскорбинова киселина (витамин С). Витамин С е добър редуктор (Ео ' = + 0.08), може да редуцира О2, нитрати и цитохроми а и с. Водно-разтворим антиоксидант, инхибира образуването на нитрозамини в храносмилателния тракт, необходим за обезвреждането на токсични свободни радикали. В организма на човек не се синтезира и трябва да се приема редовно с храната. Усвояването на желязо е по-добро в присъствие на витамин С. Участва във важни окислителни реакции, катаболитни пътища (разграждане на тирозин), в синтезни пътища (синтеза на норадреналин, образуване на жлъчка, стероидогенеза, зреене на колаген).
9.2. Синтеза на АТФ на субстратно ниво
Окислително фосфорилиране на субстратно ниво е синтезата на АТФ или други макроергични съединения за сметка на енергия, отделена при субстратно окисление.
Субстратното окисление е едностъпално анаеробно дехидрогениране на стотици различни субстрати под действие на специфични ензими дехидрогенази, кооперирани най-често с редокс-системите НАД++ и НАДФ+. В резултат значителни количества водород под форма на НАДН могат да постъпят в дихателната верига или под форма на НАДФН да се използват за редукционни биосинтези. Субстратното окисление е начален етап, предшестващ окислението в дихателната верига.
Енергията, отделена при субстратното окисление, поради малката разлика в редокспотенциалите, обикновено се разсейва като топлина, тъй като не достига за образуване на 1 мол АТФ. Известни са само три случая, когато едновременно с окислението се извършва и акумулиране на отделената енергия в макроергично съединение. Тези случаи на субстратно фосфорилиране или енергетично спрягане на субстратно ниво, са:
- окислително фосфорилиране на глицералдехид-3-Ф;
- енолазна реакция;
- окислително декарбоксилиране на α-кето киселини.
Окислителното фосфорилиране на глицералдехид-3-фосфат и енолазната реакция са част от гликолизата, протичат в цитоплазмата под действие на единични ензими. Гликолитичните фосфорилирания са важни в условия на кислородна недостатъчност. Окислителното декарбоксилиране на α-кетокиселини се катализира от дехидрогеназни комплекси и протича в митохондриите.
9.2.1. Окислително фосфорилиране на глицералдехид-3-Ф
Окислителното фосфорилиране на глицералдехид-3-фосфат се катализира от глицералдехид-3-фосфат дехидрогеназа, като коензим участва редокс-системата НАД+. Това е екзергонична реакция, при която отделената енергия не се разсейва, а се акумулира в тиоестерна макроергична връзка в рамките на ензим-субстратния комплекс. Получава се макроергичният продукт 1,3-бисфосфоглицерат, предшественик на АТФ. Макроергичната му фосфатна група се използва за фосфорилиране на АДФ до АТФ.
9.2.2. Енолазна реакция
Енолазната реакция е единствената позната реакция в биосферата, при която неорганичен фосфат се издига от нормоергично на макроергично ниво. При нея без участието на външна редокс-система, енолазата катализира дехидратиране на 2-фосфо-глицерат до предшественик на АТФ - фосфоенолпируват (ФЕП), който е с най-висока стойност на ΔGo' при хидролиза. Енол-фосфатната макроергична връзка е с ΔGo' = - 61.9 kJ/mol.
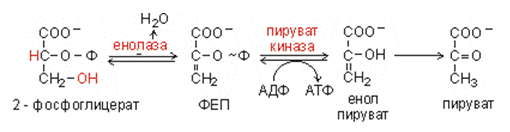
Фигура 134. Окислително фосфорилиране при енолазната реакция
Отделянето на вода е вътрешномолекулна оксидоредукция - водород се отделя от втория въглероден атом (окисление), а хидроксилна група - от третия въглероден атом (редукция).
В следващата реакция под действие на пируват киназа енергията, акумулирана в ФЕП, се използва за синтеза на АТФ, като ФЕП се превръща през енол-пируват в тавтомера пируват (кето-форма). Тавтомеризирането на енол-пируват в кето-формата е силно екзергонична реакция, чиято ΔGo' осигурява енергия, повече от необходимата за синтеза на АТФ. Това е причина за необратимостта на пируват киназната реакция.
Синтезата на АТФ от субстратните гликолитични фосфорилирания е незначителна, но разгледаните реакции имат значение, в следните случаи:
- в условия на кислородна недостатъчност са единствен източник на АТФ, напр. в усилено работещ мускул;
- не се влияят от вещества, които инхибират окислението в дихателните вериги и спрегнатото с него фосфорилиране;
- при митохондрийни заболявания снабдяват клетката с АТФ;
- доставят АТФ, когато енергията, отделена в дихателната верига, се използва не за синтеза на АТФ, а за други ендергонични процеси;
- биосинтезите в цитоплазмата се осъществяват с помощта на гликолитичен АТФ.
9.2.3. Окислително декарбоксилиране на α-кето киселини
Окислителното декарбоксилиране на α-кетокиселините пируват до ацетил-КоА и на α-кетоглутарат до сукцинил-КоА са важни реакции. Първата осъществява връзката между гликолизата и цитратния цикъл, а втората е част от цитратния цикъл.
За разлика от гликолитичните фосфорилирания, окислителното декарбоксилиране протича не в цитоплазмата, а във вътрешната митохондрийна мембрана и отделеният от субстрата водород лесно постъпва в дихателната верига. И двата случая се катализират от сложни тройни ензимни комплекси: пируват дехидрогеназен комплекс и α- кетоглутарат дехидрогеназен комплекс, които се отличават само по първия ензим в комплекса.
Организирането на ензимите в мултиензимни комплекси има предимства:
- увеличава се реакционната скорост, скъсява се разстоянието между активните центрове на ензимите, което субстратите трябва да изминат, в сравнение ако ензимите не са в комплекс;
- намалява се възможността от протичането на странични реакции, т.е. междинните метаболити да реагират с други молекули;
- по-добро координирано регулиране на реакциите, катализирани от мултиензимния комплекс.
9.3. Структура и функции на дихателната верига
9.3.1. Функции на дихателната верига
Съвкупността от преносители, разположени във вътрешната мембрана на митохондриите, които осъществяват пренасяне на електрони до крайния окислител (кислород), се нарича електронтранспортна верига или дихателна верига. Това е мултиензимна система вградена във вътрешната мембрана на митохондриите, сложно организирана и специализирана със следните функции:
- да събира редуциращи еквиваленти от различни субстрати;
- да ги пренася към О2 (окисление);
- да акумулира отделената при окислението енергия като синтезира
АТФ (окислително фосфорилиране).
При синтеза на АТФ за сметка на енергия, отделена при окисление в дихателната верига, се говори за окислително фосфорилиране или енергетично спрягане в дихателната верига.
В цикъла на лимонената киселина от субстратите се откъсват водородни атоми, които се поемат от кофакторите НАД+ и ФАД, които ги предават в дихателната верига, изградена от оксидоредуктази (намиращи се във вътрешната мембрана на митохондриите) и достигат до крайният акцептор – О2. В състава на дихателната верига се включват разнообразни химически групи, свързани с белтъци (с изключение на убихинона), които участват в преноса на електрони. Това са:
- НАД+, влизащ в състава на различни дехидрогенази;
- ФМН – свързан с НАД.Н – дехидрогеназата;
- убихинон (UQ);
- желязосъдържащи белтъци от два различни типа – желязно-серни центрове (FeS) и цитохроми.
Някои субстрати (сукцинат, мастни киселини), които не могат да се окисляват от НАД+, предават своя водород (електрони) директно на ФАД, от който чрез Fe-S-центрове се пренасят на убихинона (UQ). Реакциите на пренос на електрони, са окислително-редукционни процеси, в които съединенията, отдаващи електрони се означават като редуктори, а тези приемащи електрони, са окислители.
9.3.2. Структура на дихателната верига
Компонентите на дихателната верига, осъществяващи окислителното фосфорилиране са едно цяло с вътрешната митохондриална мембрана. Функционалната активност на системата спира, когато се нарушава
разположението на ензимите в нея, т.е. първостепенно значение има структурната организация на влизащите в нея окислително-редукционни ензими. Дихателната верига се състои от разтворими и мембранно свързани компоненти, които са организирани в 4 комплекси, действащи съвместно с АТФ синтаза. Някои от компонентите пренасят по 1 електрон (Fe-S-белтъци, цитохроми, Cu-йони). Други пренасят по 2 електрона (КоQ, ФМН, ФАД).
Електроните се придвижват от редокс-центрове с по-нисък (по- отрицателен) редокс-потенциал към редокс-центрове с по-висок (по- положителен) редокс-потенциал. В дихателната верига постъпват в резултат на действието на различни дехидрогенази. Преносът на електрони в дихателната верига е проучен подробно (със стрелки е означен потокът на електрони, фиг.135):
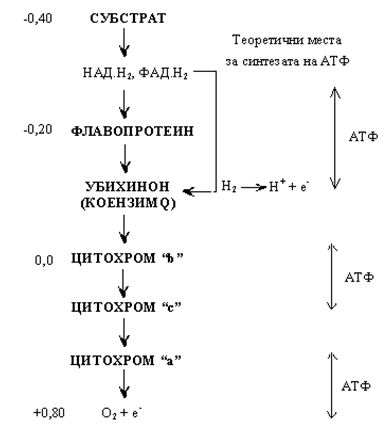
Фигура 135. Подреждане на редокс-двойките в дихателната верига
Съединенията, които участват в последователните реакции като преносвачи на електрони, постепенно увеличават окислително-редукционния си потенциал, като се започне от изходния донор на електрони и се стигне до крайния акцептор. Всеки компонент на дихателнат верига, трябва да притежава способността да се окислява и редуцира:
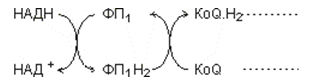
Фигура 136. Динамично преминаване на компонентите на дихателната верига от редуцирана в окислена форма и обратно
Водородът, отделен от метаболити подложени на биологично окисление, попада в дихателната верига. При окислението му в нея се отделят значителни количества енергия, която се акумулира в АТФ.
Последователният пренос на електрони по дихателната верига е гаранция за отделяне на енергията на порции, като част от нея се трансформира в богатите на енергия макроергични връзки на АТФ.
Електроните могат да навлязат във веригата от три нива:
- на ниво дехидрогеназа;
- на ниво хинони;
- на нивото на мобилния преносвач на електрони цитохром.
Дихателната верига вклюва около 40 разнообразни белтъци-преносители на електрони, които са организирани в 4 големи мембранносвързани мултиензимни комплекси. Съществува още един комплекс, който не участва в преноса на електрони, а в синтезата на АТФ.
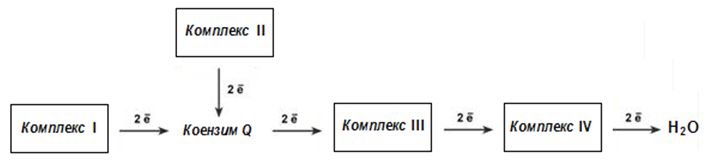
Фигура 137. Схема на дихателната верига, съставена от 4 големи мембранносвързани мултиензимни комплекси
Комплекс І. НАДН-КоQ-оксидоредуктаза. Този компрекс се нарича още НАДН–дехидрогеназа, съдържа редокс-системата ФМН като простетична група, 22 белтъчни молекули, от тях 5 Fe-S-белтъци, обща молекулярна маса до 900 kДа. Комплекс І приема два електрона от НАДН и ги пренася към КоQ (убихинон) като изпомпва 4 протона в интрамембранното пространство.
Комплекс ІІ. ФАД-зависими дехидрогенази. Този комплекс е условен. Включва флавинови дехидрогенази (ФАД-зависими ензими), които поемат електрони от субстрати с по-висок редоксипотенциал, прикрепени са към вътрешната митохондриална мембрана: ацил-SKoA-дехидрогеназа (окисление на мастни киселини), сукцинатдехидрогеназа (ЦТК), митоходриалната глицерол-3-фосфат-дехидрогеназа (совалков механизъм на пренос на НАДН в митохондриите). В техния състав също се включват желязно-серни белтъци. Комплекс ІІ пренася електрони от сукцинат през ФАД към КоQ, но отделената енергия не е достатъчна за синтеза на АТФ. Флавопротеините са ензими, които в качеството си на простетични групи съдържат флавинови нуклеотиди (ФАД, ФМН) и пренасят водород.
Двата комплекса І и ІІ предават протони и електрони на убихинона.
Хиноните са липофилни съединения, в частност убихинона и са локализирани в липофилната част на мембраната. В сравнение с другите компоненти на веригата тяхното количество е многократно повече. Те служат като “събирачи” на водород, доставян от различни коензими и простетични групи в дихателната верига, предавайки го на цитохромите. Убихинонът изпълнява колекторна функция, като събира редукционни еквиваленти не само от НАД.Н - дехидрогеназата, но и от флавиновите дехидрогенази, намиращи се в митохондриите (сукцинатдехидрогеназата и ацил-КоА дехидрогенази).
Комплекс ІІІ. КоQ-цитохром с-оксидоредуктаза. От убихинона електроните се пренасят към цитохром с, чрез ензимен комплекс познат като Убихинол:цитохром с-оксидоредуктаза. В неговият състав влизат цитохром b, един желязно-серен белтък и цитохром с1. Комплекс ІІІ пренася 2 електрона от КоQh3 към 2 молекули цитохром с, посредством Q-цикъла изпомпва 4 протони в интрамембранното пространство.
Цитохромите вземат участие в заключителния етап на веригата, при пренасянето на електрони. Те не пренасят водород. При пренасянето на електрони, еквивалентен брой протони преминават в разтвора. Цитохромите са белтъци, които съдържат железопорфиринови простетични групи.
Централния атом на желязото изменя валентността си при пренасянето на електроните:
Fe2+ ↔ Fe3+ + e-
Цитохромите са оцветени в червено или кафяво. Те действат в определена последователност и пренасят електрони от убихинола на молекулния кислород. Познати са три вида цитохроми – a, b, c, които се различават по спектъра на поглъщане.
Комплекс ІV. Цитохром с-кислород-оксидоредуктаза. Последният ензимен е изграден от цитохромите а и а3, и е познат като цитохромоксидаза. Тази ензимна система е съставена от 6 до 13 субединици и два куприйона. Комплекс ІV редуцира О2 до 2h3О като използва 4 електрона от цитохром с и 4 протона от матрикса. За всеки 2 електрона, които редуцират кислород, се изпомпват в интрамембанното пространство 2 протона.
Комплекс V. Ензим АТФ-синтаза. Състои се от множество белтъци, разделени на две големи групи, формиращи:
- субединица F0 – функцията, която изпълнява е каналообразуваща, по нея изпомпените в междуклетъчното пространство протони на водорода се връщат в матрикса;
- субединица F1 – каталитична функция, използва енергията на протоните за синтеза на АТФ (фиг.140).
Счита се, че за синтезата на 1 молекула АТФ е необходима преминаването на приблизително 3 протона Н+. Количествен израз на сродството към електроните, т.е. на способността към окисление (респ. редукция) се дава от стойността на редоксипотенциала, означаван като Ео. При биологичните редоксисистеми той се измерва при рН 7 и се бележи с Ео´. Колкото по-висока е стойността на отрицателния редоксипотенциал на една система толкова по-висока е способността й да отдава електрони и обратно, колкото по-висок е положителния редоксипотенциал, толкова по-голяма е способността на системата да приема електрони.
Таблица 5. Редоксипотенциали на определени реакции
Полуреакции |
E o' (Volts) |
Цитохром a (Fe3+) + e- --> (Цитохром a (Fe2+) |
0.29 |
Цитохром b (Fe3+) + e- --> Цитохром b (Fe2+) |
0.077 |
Цитохром c (Fe3+) + e- --> Цитохром c(Fe2+) |
0.254 |
Цитохром c1 (Fe3+) + e- --> Цитохром c1(Fe2+) |
0.22 |
FAD + 2H+ + 2e- --> FADh3 |
-0.219 |
Fe3+ + e- --> Fe2+ |
0.771 |
2H+ + 2e- --> h3 (в стандартни условия, pH 0) |
0.00 |
2H+ + 2e- --> h3 (при pH 7, биохимичен стандарт) |
-0.414 |
NAD+ + H+ + 2e- --> NADH |
-0.320 |
NADP+ + H+ + 2e- --> NADPH |
-0.324 |
1/2 O2 + 2H+ + 2e- --> h3O |
0.816 |
Убихинон + 2H+ + 2e- --> Убихинол + h3 |
0.045 |
В дихателната верига всички реакции са в посока от компонента с максимално отрицателен редоксипотенциал НАД.Н (-0,32V) към кислорода, имащ най-голям положителен редоксипотенциал (+0,82V). Следвайки този принцип, компонентите на дихателната верига се разполагат в определен ред. Движението на електроните от една редоксисистема към друга е свързано с намаляване на свободната им енергия. Колкото по-голяма е разликата в стандартните потенциали на две редоксисистеми, толкова повече се понижава свободната енергия. Намаляването на свободната енергия, на всеки етап от преноса в електронната верига, може да се представи чрез следната диаграма:
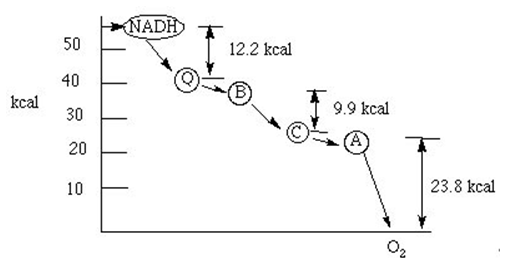
Фигура 138. Намаляване на свободната енергия, на всеки етап в електронната верига
Преминавайки през цялата верига от междинни преносители от НАД.H (Eо´=-0,32V) към кислорода (Eо´=+0,82V) електроните губят значително количество свободна енергия. Тя може да се определи по формулата:
∆Gº´= - nFΔΕ○´,
където:
Y ∆Gº´- изменение на свободната енергия, kJ;
Y n – числото на пренесените електрони;
Y F – константа, наричана числото на Фарадей (96,5 kJ)
Y ΔΕ○´ - разлика между редоксипотенциалите на акцептора и донора на електрони, V.
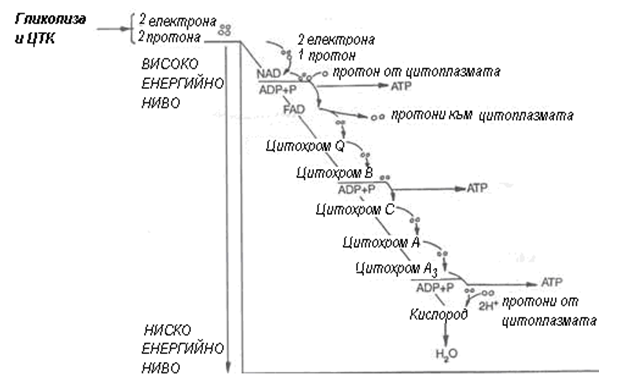
Фигура 139. Дихателна верига, намаляване на свободната енергия и окислително фосфорилиране
Механизмът на образуването на АТФ все още не е окончателно изяснен. Приема се, че процеса се катализира от АТФ-синтезата (F1Fо-ATФ-аза). Това е един трансмембранен протеин, който се състои от два основни компонента – Fо и F1. Те от своя страна са изградени от голям брой субединици (α, β, γ, δ, ε и др.).
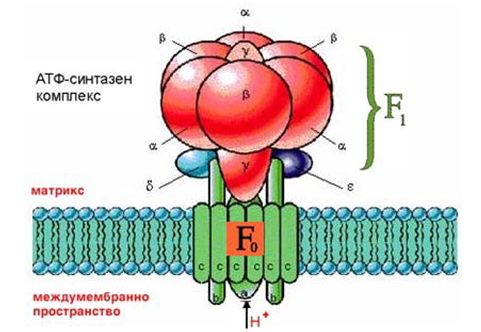
Фигура 140. Структура на АТФ синтазен комплекс.
Компонентът F1 се състои от 9 субединици от 5 различни типа α, β, γ, δ, ε. Субединиците α и β оформят главичка, а останалите - крачето. Компонентът Fo е разположен в мембраната. В него се свързва олигомицин и блокира преноса на водород през ензима, а с това и окислителното фосфорилиране..
9.3.3. Механизъм на окислително фосфорилиране в дихателните вериги
Синтезата на АТФ включва:
Y поемане на протони от Fo от междумембранното пространство и пренос към F1;
Y синтеза на АТФ под действие на F1;
Y използване на енергията на протонния градиент за освобождаване на
АТФ от Fо, което изисква взаимодействие между Fo и F1.
Съществуват няколко хипотези за синтезата на АТФ, най-правдоподобна изглежда хими-осмотичната теория на Митчел или електрохимичната хипотеза. Според нея преносът на електрони се съпровожда с “изкачване” на протони от матрикса към междумембранното пространство на митохондриите. Създава се протонен концентрационен градиент от двете страни на вътрешната митохондриална мембрана (трансмембранен градиент, фиг.141, 142). Енергията отделена от окислението на НАД.H се улавя в началото като протонен градиент на вътрешната митохондрийна мембрана (фиг.142). Синтезата на АТФ, изискваща загуба на енергия, се осъществява за сметка на осмотичната енергия, присъща на този градиент.
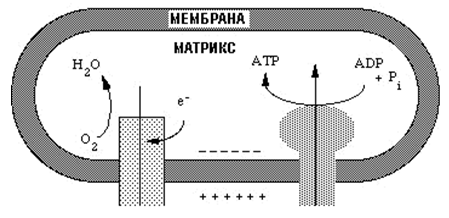
Фигура 141. Протонен градиент
Този градиент се използва от ензима (АТФ-синтаза) за осъществяване на синтеза на АТФ. Например при преминаването на два електрона през дихателната верига към О2, ∆Gº´=-220kJ. Това количество енергия е достатъчно за синтезата на няколко молекули АТР. От горната формула може да се пресметне, че за синтеза на молекула АТР (∆Gº´=-34,5 kJ) е достатъчна разлика в редоксипотенциалите от 0,20 – 0,25 V. Въз основа на това условие е доказано, че в дихателната верига се образуват три молекули АТР – между НАД и UQ (убихинона); между цит. „b“ и цит.“с“; и между цит.“a“ и кислорода.
Митчел постулира и разработва схема за механизма на окислителното фосфорилиране, в дихателните вериги:
Y митохондрийната мембрана е непроницаема за H+ и -ОН;
Y дихателни преносители, трансмембранно ориентирани осъществяват векторен пренос на електрони и протони през мембраната;
Y АТФазна система пренася протони и синтезира АТФ.
Преносът на електрони по дихателната верига към О2 е движеща сила за изнасяне на протони от матрикса към междумембранното пространство (фиг. 142). Комплекс І, комплекс ІІІ и комплекс ІV, не синтезират директно АТФ, а действат като протонни помпи, пренасяйки електрони към кислорода изпомпват протони от матрикса в интрамембранното пространство. Това формира трансмембранен електрохимичен потенциал, с две компоненти - химична (натрупва Н+ отвън и ОН- вътре в матрикса) и електрична (натрупва положителни заряди в междумембранното пространство и отрицателни заряди в матрикса). Този електрохимичен потенциал, неговата енергия се използва за синтеза на АТФ от АТФ синтазата. Доказано е експериментално, че рН в междумембранното пространство е по-ниско, отколкото в матрикса.
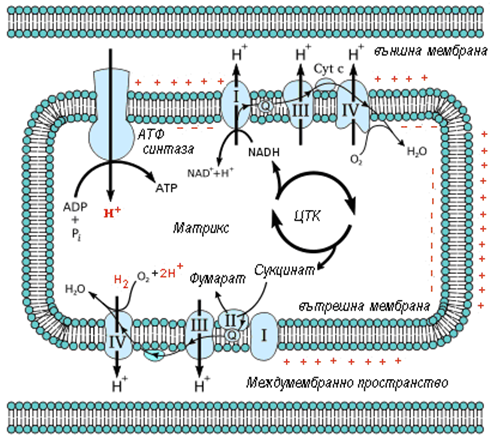
Фигура 142. Механизъм на окислителното фосфорилиране в митохондрийната мембрана, според химио-осмотичната теория на Митчел
Комплексите I, III и IV, действат като протонни помпи, изпомпват протони от матрикса в междумембранното пространство, възниква трансмембранен електрохимичен потенциал. Тъй като мембраната е непропусклива за протони, връщането им в матрикса става по градиента, но само през молекулния комплекс на АТФ-синтазата. Преходът на протони от зона с висока концентрация на протони към зона с ниска концентрация отделя свободна енергия, за сметка на която се синтезира АТФ. Така между матрикса и междумембранното пространство се извършва непрекъснат кръговрат на протони, движеща сила на който е транспортът на електрони.
9.3.4. Принцип на работа на дихателните вериги
Работата на дихателните вериги може да обобщи като:
1. Образуваните в реакциите на катаболизма редуцирани НАДН и ФАДН2 предават атомите водород (протони и електрони) на ензимите на дихателната верига;
2. Електроните се движат по веригата от редокс-системи и губят енергия;
3. Тази енергия се използва за извеждане на протони Н+ от матрикса в междумембранното пространство;
4. Краен акцептор на електроните в дихателната верига е кислорода и се образува вода;
5. Протоните Н+ се стремят да се върнат в матрикса и преминават през АТФ-синтазата;
6. При това те губят енергия, която се използва за синтеза на АТФ.
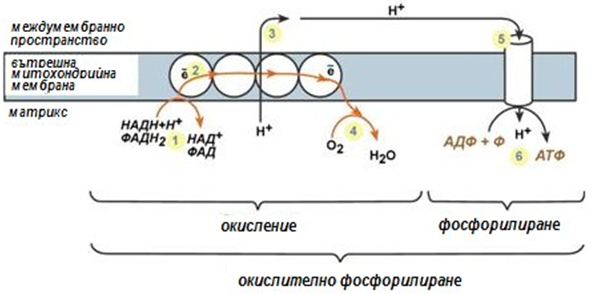
Фигура 143. Общи принципи на работа на дихателните вериги
9.4. Ефективност на окислението. Коефициент на окислително фосфорилиране (Р/О)
Коефициентът на окислителното фосфорилиране (Р/О) показва колко мола АТФ се синтезират от АДФ и Ф при транспорт на два електрона към един атом кислород до получаване на вода в дихателната верига. Коефициента Р/О е съотношението на количеството неорганичен фосфат включен в молекулата АТФ от АТФ-синтетазата към количеството атоми кислород, включени в молекулата Н2О, при пренос на една двойка електрони по дихателната верига.
Експериментално е установено, че при окисление на вещества с участие на НАД-зависима дехидрогеназа, съотношението на количеството включен фосфат в АТФ, се отнася към количеството използвани атоми кислород като 3:1, т.е. коефициента Р/О е равен на три. Аналогично за ФАД-зависимите дехидрогенази коефициента Р/О е равен на две. Теоретично изпомпването на 10 протони при преноса на електрони от НАДН към кислород е достатъчно за синтез на 3 мола АТФ. При пренос на електрони от сукцинат през ФАД се изпомпват 6 протони, което е достатъчно за синтеза на 2 мола АТФ. Преносът на 2 електрона през комплекс ІV изпомпва 2 протона, достатъчно за синтеза на 1 мол АТФ.
Коефициентът на окислително фосфорилиране Р/О, не е задължително да бъде цяло число. Експериментално определяните стойности на Р/О не са цели числа, а са 2.5, 2 и 1, съответно за пренос на електрони от комплекс І до О2, комплекс ІІ до О2 и комплекс ІV до О2.
Енергетичната ценност и изгодност от окислението на веществата може да се изчислява. Количеството на съхранената енергия при окислението на едно или друго вещество се характеризира с количеството синтезиран АТФ, а ефективността от използване на енергията и нейното улавяне от коефициента Р/О. При изчисляване енергетичната ценност, т.е. количеството синтезиран АТФ образувани при окислението на субстрата и коефициента Р/О, е необходимо да се отчете целия метаболитен път на веществото до пълното окисление на въглеродните му атоми до СО2. При това е необходимо да се отчита броя на въглеродните атоми в молекулата.
При изчисляване Р/О на коя да е молекула, е необходимо да се отчита:
Y НАДН и ФАДН2 пренасят по два електрона в електронтранспортната верига;
Y за въвеждането на кислород в молекула вода е необходима двойка електрони;
Y при преминаването на двойка електрони през дихателната верига се отделят толкова йони Н+, колкото са необходими за синтезата на 3 молекули АТФ, или в състава на АТФ се включват три атома неорганичен фосфат;
Y при преминаването на двойка електрони през III и IV комплекс на дихателната верига се отделят толкова йони Н+, колкото са необходими за синтезата на 2 молекули АТФ, или в състава на АТФ се включват два атома неорганичен фосфат;
Пример: Изчисляване на коефициента на окислително фосфорилиране (Р/О) за аспартата - начало на отчитането започва с оксалацетата, който се образува от трансаминирането на аспартата, отчитането завършва също на това ниво. Оксалацетат съдържа 4 атома въглерод и затова е необходимо да премине 2 оборота от ЦТК, преди да отдели този въглерод като СО2. Отчитаме редуцираните НАДН, ФАДН2 образувани от двата оборота на ЦТК и определяме крайната сума на АТФ – 24 молекули. При пресмятането на коефициента Р/О отчитаме единствено фосфата, който е включен в АТФ от ензима АТФ-синтетаза, т.е. в процеса на окислително фосфорилиране. Това означава, че фосфата влизащ в ГТФ, не се отчита.
Всяка молекула редуцирана НАДН или ФАДН2 предава на дихателната верига по една двойка електрони, които преминават различно разстояние: от НАДН – три ензимни комплекса, при ФАДН2 – два ензимни комплекса, но внасят един атом кислород в молекула вода. При окислението на НАДН се образуват 3 молекули АТФ, при окислението на ФАДН2 – 2 молекули АТФ.
9.5. Свободно окисление
9.5.1. Свободно окисление и топлопродукция
При свободното или неспрегнато окисление, отделената енергия не се акумулира в макроергични съединения, а се превръща в топлина, което е важно за поддържане на постоянна телесна температура в топлокръвните организми. За разлика от бялата мастна тъкан, в кафявата мастна тъкан се съдържа по-голямо количество митохондрии, които придават на клетките кафяв оттенък. Във вътрешната мембрана на митохондриите има белтък термогенин (до 15% от всички белтъци на митохондриите), през който изпомпаните в интрамембранното пространство протони се връщат в матрикса, но не преминават през АТФ-синтазата (фиг.144). Чрез термогенин, вместо за синтеза на АТФ, енергията на протонния градиент се превръща в топлина.
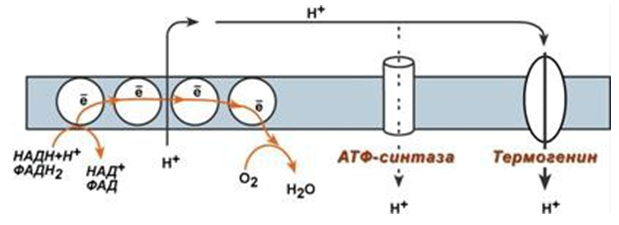
Фигура144. Действие на разпрягащия белтък термогенин в митохондрии
Дихателната верига изпомпва протони от матрикса в междумембранното пространство. Вместо през АТФ-синтетазния комплекс, протоните се връщат обратно в матрикса през термогенин, който осигурява алтернативен път. Така вместо за синтеза на АТФ, енергията на протонния градиент се разсейва като топлина, т.е. използва се за топлопродукция.
Под влияние на студ от студовите рецептори по кожата се изпраща сигнал в централната нервна система, откъдето се сигнализира за отделяне на хормона адреналин, който активира липазата в мастна тъкан. Липазата разгражда мастите до висши мастни киселини (ВМК) и глицерол. ВМК действат разпрягащо върху митохондрийните дихателни вериги в мускулите. Митохондрийните дихателни вериги в мускулите и мастната тъкан се разпрягат от повишено съдържание на висши мастни киселини, отделени от триацилглицероли под въздействие на адреналин, който активира липаза в мастна тъкан. В повечето бозайници, вкл. и човека, при новородени има особена кафява мастна тъкан, чиято главна задача е да продуцира топлина за бебето. Тя е разположена отзад на врата на бебетата. Кафявият цвят идва от присъствието на голям брой митохондрии, и следователно голямо количество цитохроми, чиито хемни групи силно поглъщат видима светлина. В кафявата мастна тъкан митохондриите са практически винаги разпрегнати поради високите концентрации на висши мастни киселини. Спящите зимен сън животни (кафяви мечки, мечки-гризли) също имат големи количества от тази тъкан.
9.5.2. Метаболитно значение на свободното окисление
В ендоплазмения ретикулум има скъсени електронопреносителни вериги, които се отличават от дихателните вериги в митохондриите по локализация, компоненти и функция.
Вместо НАД, НАДФН е донатор на Н. Вместо цитохроми участват други цитохроми, цит.Р450, цит.в5. В тях не се произвежда АТФ и топлопродукция, а се извършва десатурация или получаване на ненаситени мастни киселини, или хидроксилиране на субстрати.
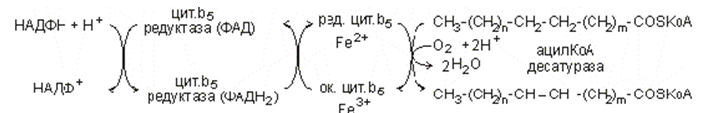
Фигура145. Скъсена електронпреносна верига за десатурация на висши мастни киселини, под форма на активни ацил-КоА.
Водородните атоми от мастната киселина редуцират единия кислороден атом. Водородните атоми от НАДФН + Н+ редуцират другия кислороден атом.
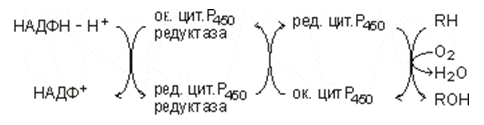
Фигура 146. Скъсена електронпреносна верига за хидроксилиране на субстрати
Единият кислороден атом се използва за получаване на -ОН група, а другият не остава свободен, а се редуцира от водорода на НАДФН + Н+, пренесен по веригата.
В черния дроб се извършва неспецифично хидроксилиране на всякакви чужди за клетката вещества с цел обезвреждането им. Някои от тях, първоначално безвредни, след хидроксилирането се превръщат в мощни
канцерогени. В бъбреците и черния дроб се извършва хидроксилиране,
необходимо за превръщане на вит. D2 в активния хормон калцитриол. При синтеза на жлъчни киселини в черния дроб също се извършва специфично хидроксилиране. В стероидогенните тъкани (адренален кортекс, тестиси, яйчници, плацента) се извършва специфично хидроксилиране като етап от синтезата на стероидни хормони (мъжки и женски полови хормони, а също минерал- и глюкокортикоиди).
Терминологичен речник
#Окислително фосфорилиране - процес, при който АТФ се синтезира при пренасянето на електрони от НАДH или ФАДh3 до O2, чрез поредица от електронни преносители. Окислителното фосфорилиране се осъществява във вътрешната митохондрийна мембрана.
# Субстратно окисление - едностъпално анаеробно дехидрогениране на различни субстрати под действие на специфични ензими дехидрогенази, кооперирани най-често с редокс-системите НАД++ и НАДФ+. В резултат значителни количества водород под форма на НАДН могат да постъпят в дихателната верига или под форма на НАДФН да се използват за редукционни биосинтези.
#флавопротеини - ензими, които в качеството си на простетични групи съдържат флавинови нуклеотиди (ФАД, ФМН). Те пренасят водород.
#коефициент на окислително фосфорилиране Р/О – показва колко мола АТФ се синтезират от АДФ и Ф при транспорт на два електрона към един атом кислород до получаване на вода в дихателната верига.
#свободно окисление - отделената от окислението енергия не се акумулира в макроергични съединения, превръща се в топлина, което е важно за поддържане на постоянна телесна температура в топлокръвните организми.




